バイオ医薬品生産で操作された細胞に由来する宿主細胞タンパク質 (HCP) は、製品の品質、有効性、および安全性に影響を与える可能性があります。 したがって、HCPモニタリングは、製造プロセスにおける重要な品質属性 (CQA) を構成します。 HCPの多様性が非常に高いことを考えると、グローバルな規制基準を満たすには、複数の検出および識別技術が必要です。
1. HCP分析および検出技術プラットフォーム (ELISA、LC-MS & 2D)
A.深セン®HCP ELISAキット正確でターゲットを絞った検出を確実にするために、特定の手法にカスタマイズされています。
B.アッセイの精度および信頼性を保証するためのHCP ELISA標準トレーサビリティシステム。
C。プロセス固有および高リスクのHCPと、前臨床および臨床試験ロットなどのバッチ間のHCPの変動を正確に評価します。
D.バイオプロセス開発のHCP ELISA制限を補足するために直交技術を使用して高リスクのHCPを特定します。
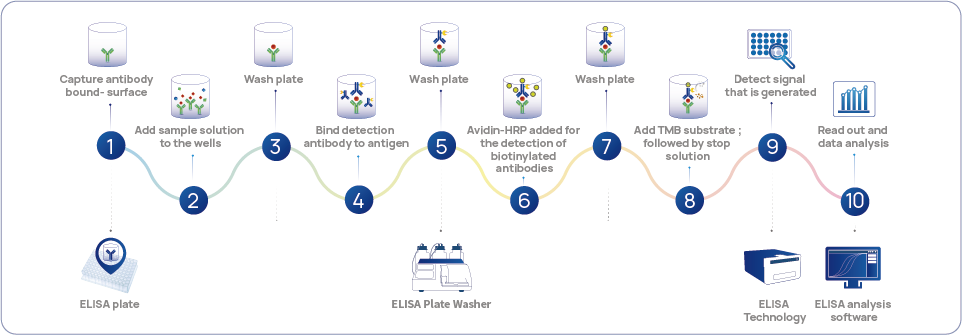
図1 HDP標準技術-ELISA検出ワークフロー
2. HCP抗体カバレッジ解析プラットフォーム (IMBS-2DおよびIMBS/LC-MS)
A.IMBS®(免疫磁気ビーズ分離) 特定の抗原を迅速に分離するための抗原-抗体-磁気ビーズ免疫複合体に基づく技術。
B.2DおよびLC-MSは、抗体とHCPの間の一致度の多角度、正確、および客観的表現を提供します。
C.HCP抗体の特異性は、シミュレートされたプロセスサンプルまたは初期段階のプロセスサンプルのカバレッジ分析によって測定されます。
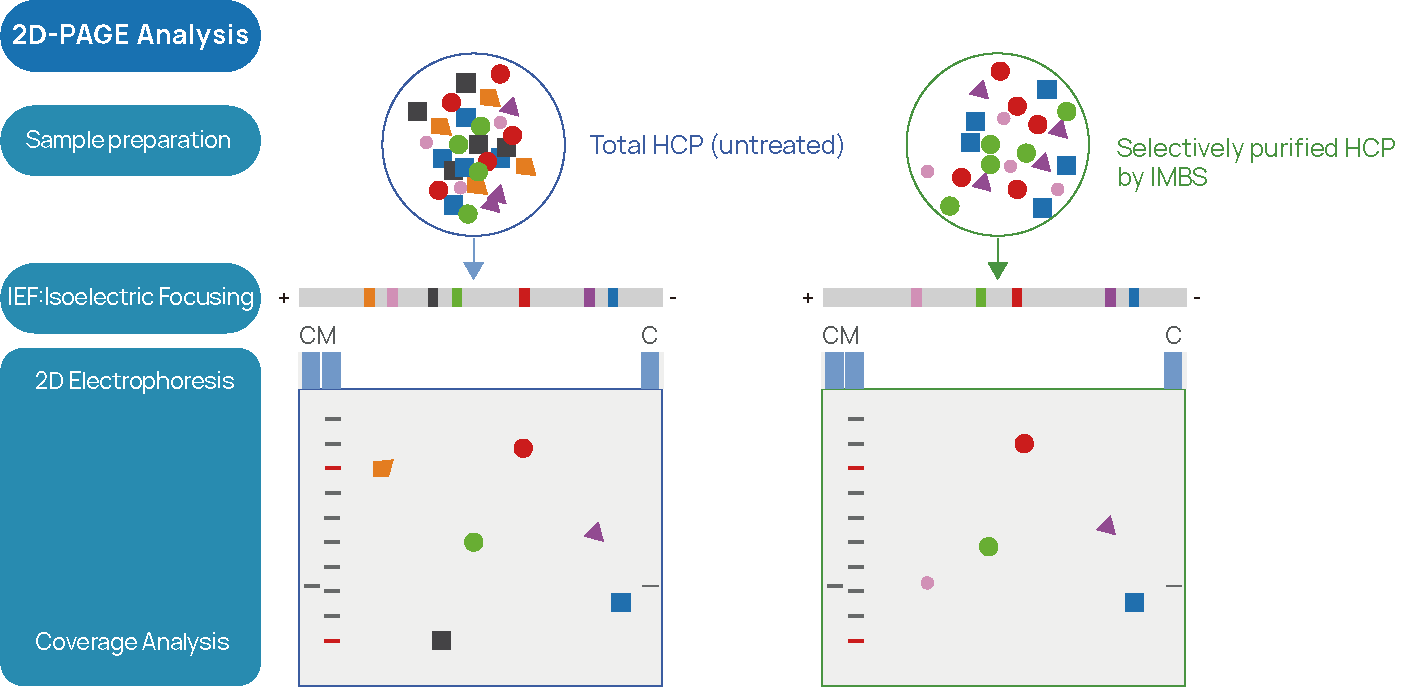
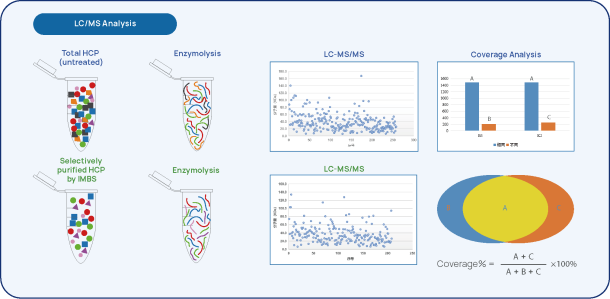
図2 IMBS-2DとIMBS-LC/MS HCP-抗体カバレッジ分析
3. HCPポリクローナル抗体准备プラットフォーム
A.異なる抗原のための免疫経路および戦略をカスタマイズする。
B.プロセス全体を通して、正確な抗体特性を有する高品質抗体の準備をモニターする。
C.高い被覆率および有効性を有する抗体の生成を確実にするためのマルチモード標準化抗体調製プラットフォーム。
D.HCPの参照プロダクトのトレーサビリティシステムを通して検出システムの信頼性および比较可能性を保障して下さい。
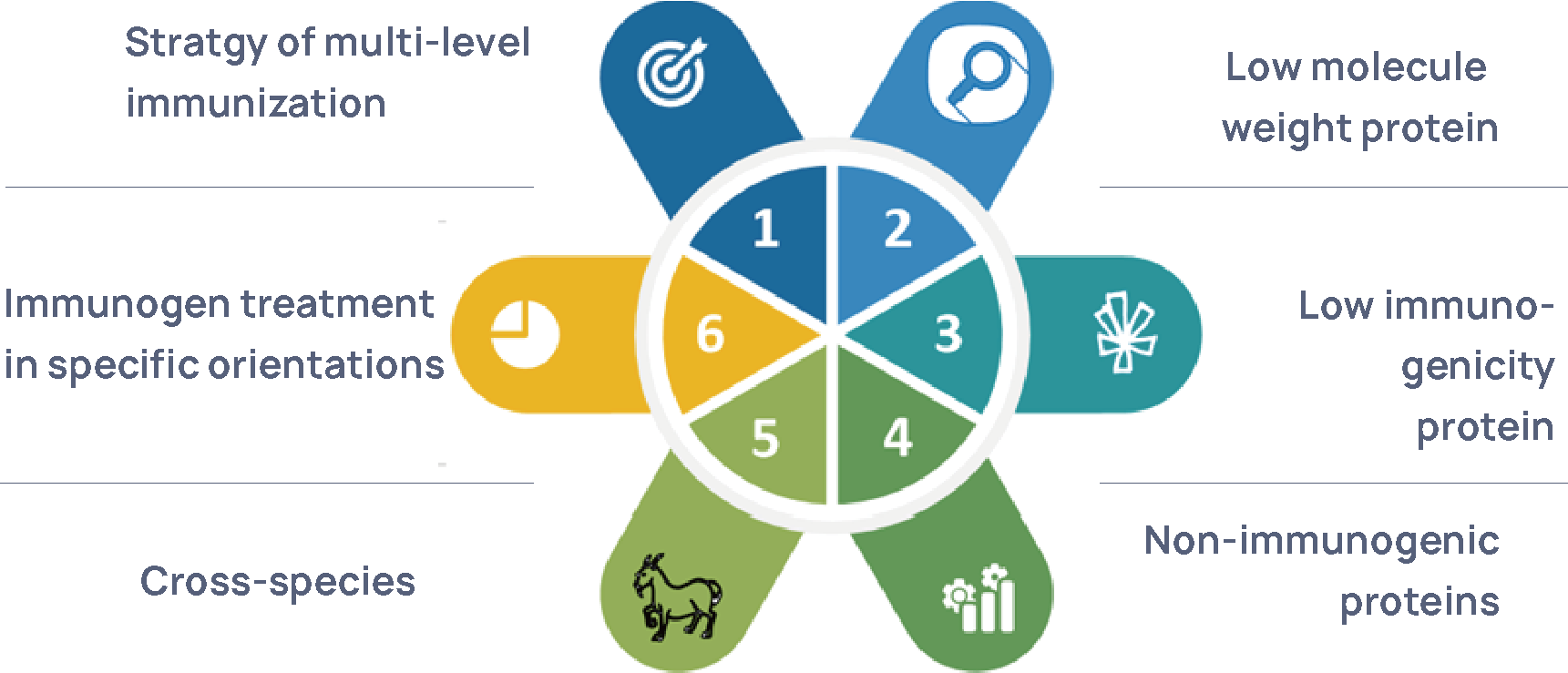
図3 HCPポリクローナル抗体调制プラットフォーム
4. Customized HCP ELISAキットプラットフォーム
A.優れたカバレッジと特異性を達成するための残留HCP (rHCP) 標準の包括的な研究。
B.イムノアッセイの信頼性を確実にするためのHCP参照トレーサビリティの標準的な実践。
C。強力な免疫応答と高品質のポリクローナル抗体のための効果的で集中的な抗原および抗体調製戦略。
D.高品質のHCP ELISAキット開発を保証するISO13485品質システムの遵守。
E.サービスと製品の整合性を確保するためのCNAS/ISO10725とGMP品質基準の遵守。
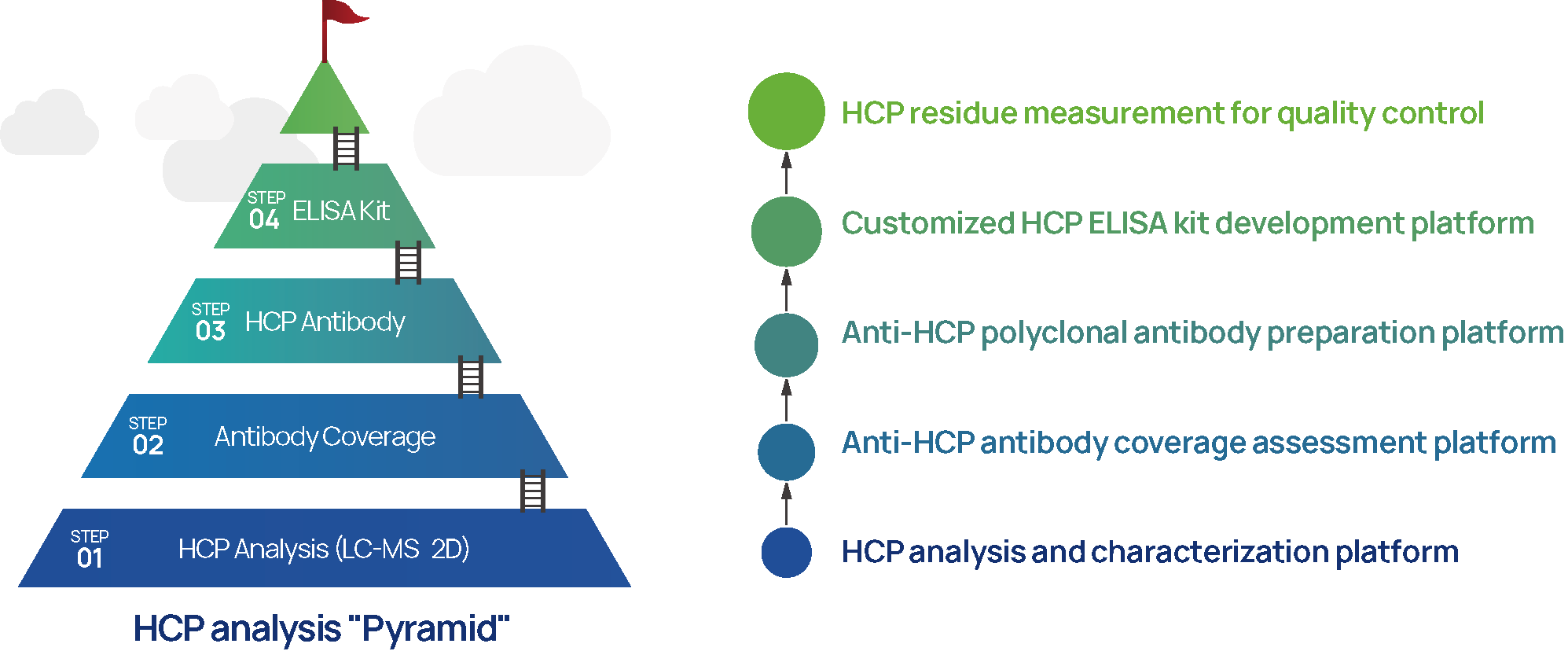
図4: SHENTEK残留宿主細胞タンパク質分析サービスプラットフォーム