生物製剤は、細菌、酵母、動物細胞、および連続細胞株の宿主から発現されます。 生物学的生成物は細胞基質から生成されるため、最終生成物に残留宿主細胞DNAが存在することは避けられません。 それは、通過細胞株の腫瘍またはウイルス関連遺伝子のために、免疫原性、発癌性、および感染性の潜在的なリスクを持っています。 残留DNAは、安全性に対する潜在的に高いリスクを有し、重要な品質属性と考えられる。 WHO、EU、およびFDAを含む現在の機関は、許容される残留DNAの量を制限していました (10 ngまたは100 pg/用量未満)。 残留DNAを検出する方法の中で、qPCRは、その感度、精度、精度、および時間の節約のために、残留DNAの定量に最も実用的であると考えられています。
RDNAは多種多様な宿主に由来する可能性があるため、rDNAはさまざまなサイズと物理的形態で存在する可能性があります。DNA含有量とサイズのさまざまな制限は、科学的証拠と堅牢なリスク評価によってサポートされている場合、規制当局に受け入れられる可能性があります。 宿主細胞のDNA残基のレベルは、製品の一貫性と品質管理の指標として役立ちます。 残留DNAを検出すると、生産バッチ間の一貫性が保証され、製品の品質評価の参考資料が提供されます。
宿主細胞のDNA濃度とサイズ分布を分析するために、最初にサンプルからDNA画分を抽出して、サンプルマトリックスからの阻害化合物なしで検出を確実にします。 磁気ビーズ分離は、この目的のために最も一般的に使用される技術であり、スループットと精度を向上させる自動抽出プロセスを可能にします。
残留宿主細胞DNAの抽出効率を決定するために、抽出前に既知の量の標的DNA (「スパイク」) をサンプルに加える。 抽出後に測定されたDNA量をスパイク量と比較することにより、抽出効率を算出することができる。 次いで、この効率値を用いて、サンプル中の残留宿主細胞DNAを決定する。 抽出効率の低下は、核酸と共抽出された阻害化合物の存在を示す。
リアルタイムPCRを使用して宿主細胞DNAの高感度で特異的な検出方法を開発するには、注意深いプライマー設計とPCR反応の最適化が必要です。 の特异性と感度リアルタイムPCRアニーリング温度、時間、および反応バッファー中のカチオンとプライマーの濃度の影響を受けます。 複数のコピーに存在する遺伝子を標的とすると、アッセイ感度を高めることができます。
アッセイ法の直線性と範囲は、標準曲線の回帰線を計算することによって評価されました。 精度は、3つの異なる濃度でスパイクされたDNA標準の回収率を分析することによって評価されました。 アッセイ内およびアッセイ間の精度は、各レベルにおけるすべてのQCの % CVを介して評価した。 感度は、LODおよびLLOQをチェックすることによって決定した。 特異性は、関連する種/株から抽出されたDNAサンプルまたはマトリックスDNAのプールを分析することによって評価した。 堅牢性は、異なる保存条件下でのアッセイ性能の安定性を評価することによって評価した。
残留宿主細胞DNAアッセイの検証範囲は次のとおりです。
精度
精度
特異性
定量の限界 (LOQ)
直線性
範囲
丈夫さ
完全に検証されたアッセイにより、市販の製品または宿主DNA配列を標的とする特別に設計されたキットの使用が可能になり、生物学的製品間のテストに適用できます。
ケーススタディ-残留宿主細胞DNA定量
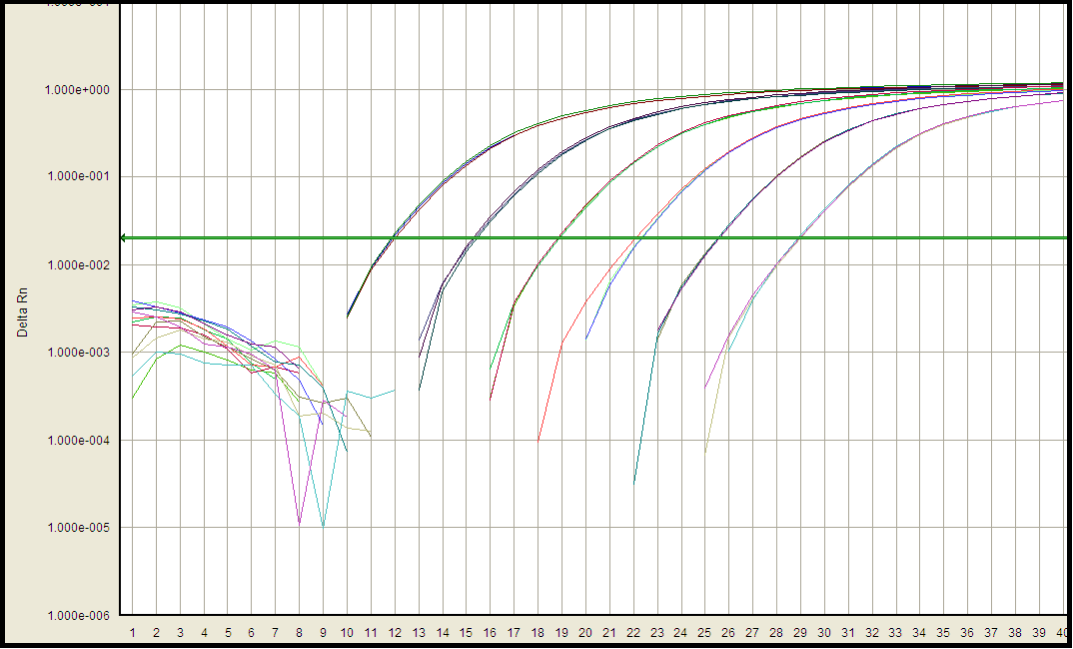
CHO HCD検証パフォーマンス-
標準曲線: 増幅効率96.6% 、相関係数0.999